BİYOEŞDEĞERLİK
Dünya çapında tanınmış ve çalışmaları FDA ve EMEA tarafından onaylanarak
güvenilirliği kanıtlanmış araştırma kuruluşları ile işbirliği içinde yapılan
klinik çalışmalar sonunda bugün EİS'in Türkiye pazarındaki tüm ürünlerinin
biyoeşdeğerlikleri Avrupa standartlarına uygun olarak tamamlanmıştır.
Kuruluşumuz yeni geliştirdiği ürünlerin biyoeşdeğerlik çalışmalarını da aynı
titizlikle sürdürmektedir.
Biyoeşdeğerlik orjinal ilaç ile aynı aktif maddeyi içeren, aynı molar doza ve
benzer bir formülasyona sahip olan bir ilacın biyoyararlanımının orijinal
ilacın biyoyararlanımı ile benzerliğinin tanımlanmış istatistiksel kriterlerle
gösterilmesidir.
En basit anlamda biyoyararlanım; verilen dozun sistemik dolaşıma geçme yüzdesi
olarak ifade edilebilir. Biyoyararlanım aktif maddenin ilacın uygulama yerinden
emilerek vücüttaki etki yerine ulaşma hızı ve derecesi olarak bilinir.
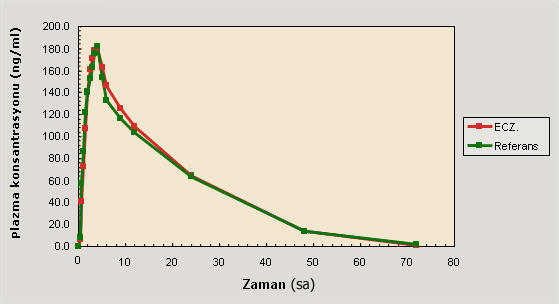
Biyoyararlanımların karşılaştırılmasında birinci derecede önemli iki
farmakokinetik parametre vardır. Bunlar AUC (Konsantrasyon-zaman eğrisi altında
kalan alan) ve Cmax (İlacın kandaki en yüksek konsantrasyonu) parametreleridir.
Merkezi otoriteye sunulabilecek en güçlü araç
Etkinlik ve güvenliği kanıtlanmış orijinal bir ilaç ile aynı etken maddeyi
içeren, aynı doza ve benzer bir formülasyona sahip olan ancak farklı bir
kuruluş tarafından üretilen yeni bir ilacın merkezi otorite tarafından
onaylanıp pazarlanabilmesi için orijinal ilacın gösterdiği etkinlik ve
güvenliği göstermesi şarttır.
Buradaki temel varsayım iki farklı üretici tarafından aynı fiziksel ve kimyasal
özelliklere sahip iki ilacın aynı düzeyde plazma konsantrasyonu oluşturmaları
durumunda ilacın etki yerindeki konsantrasyonlarının da aynı olacağı,
dolayısıyla etkinlik ve güvenlik açısından sözkonusu iki ilaç arasında fark
olmayacağıdır.
 |